Valsartan
Chất ức chế thụ thể Angiotensin II độ tinh khiết cao để điều trị tăng huyết áp
GTIG Guomian là nhà cung ứng đáng tin cậy của bạn Nhà cung cấp nguyên liệu Valsartan và đối tác chiến lược. Chúng tôi chuyên cung cấp nguyên liệu Nguyên liệu ức chế thụ thể Angiotensin II độ tinh khiết cao tuân thủ Tiêu chuẩn dược điển USP/EP , phù hợp với thuốc chống tăng huyết áp và sản phẩm điều trị tim mạch phát triển.
Sản phẩm của chúng tôi có nguồn gốc từ các cơ sở cGMP được chứng nhận, đi kèm đầy đủ Tài liệu Valsartan DMF , đảm bảo nguồn cung ổn định cho các thị trường toàn cầu.
- Tổng quan
- Sản phẩm đề xuất
- Đảm bảo chất lượng: Kiểm soát nghiêm ngặt theo hệ thống chất lượng cGMP của chúng tôi, với sự chú ý đặc biệt đến việc kiểm soát tạp chất nitrosamine (ví dụ: NDMA) , đảm bảo tiêu chuẩn an toàn và độ ổn định chất lượng cho từng lô sản phẩm.
- Năng lực sản xuất ổn định: Chúng tôi có các đối tác sản xuất đáng tin cậy và chuỗi cung ứng được tối ưu hóa, hiệu quả đảm bảo dài hạn, ổn định việc cung ứng API tim mạch quan trọng này. (Công suất sản xuất hàng năm vượt quá 400 tấn)
- Tính linh hoạt về thông số kỹ thuật: Chúng tôi cung cấp nhiều quy cách khác nhau từ 100g cấp nghiên cứu và phát triển, mẫu 1kg đến đóng gói thương mại 25kg, đáp ứng nhu cầu ở các giai đoạn khác nhau của bạn từ nghiên cứu và phát triển đến sản xuất thương mại.
- Tài liệu Kỹ thuật Đầy đủ: Mỗi lô hàng của sẢN PHẨM đi kèm báo cáo chi tiết về Giấy chứng nhận phân tích (COA) và Phiếu dữ liệu an toàn vật liệu (MSDS) , bao gồm kết quả xét nghiệm tạp chất nitrosamine .
- Hỗ trợ Tài liệu Đăng ký: Chúng tôi có thể cung cấp cho các đối tác đủ điều kiện phần mở của tài liệu DMF/EDMF cần thiết cho việc đăng ký thuốc tại Hoa Kỳ, EU và các thị trường quốc tế khác, giúp đẩy nhanh đáng kể quá trình đăng ký sản phẩm của bạn.
- Tư vấn Quy định: Đội ngũ chuyên trách về quy định của chúng tôi có thể cung cấp tư vấn về các yêu cầu quy định mới nhất đối với thuốc nhóm sartan tại các thị trường mục tiêu (ví dụ: Brazil ANVISA, Ấn Độ CDSCO).
- Hợp tác với các công ty hậu cần hóa chất chuyên nghiệp, phủ sóng các thị trường trọng điểm như châu Âu, châu Á - Thái Bình Dương và Mỹ Latinh.
- Thành thạo thủ tục thông quan, cung cấp dịch vụ theo dõi hàng hóa toàn trình và cam kết giao hàng.
1. Tóm tắt Sản phẩm Chính
|
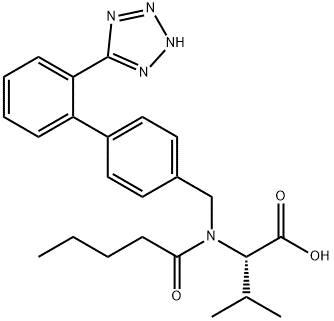
Tên sản phẩm: Valsartan CAS No.: 137862-53-4 Công thức phân tử: C ₂₄ H ₂₉ N ₅ O 3 Cân tử: 435.52 |
 |
Cấp độ/Tiêu chuẩn: Loại dược phẩm, Đạt tiêu chuẩn USP/EP
Hình thức: Bột tinh thể màu trắng đến trắng ngà
Số lượng đặt hàng tối thiểu: 100g (nghiên cứu và phát triển), 1kg (mẫu), 25kg (đơn hàng thương mại, hỗ trợ LCL)
2. Tổng quan sản phẩm
Valsartan là một lõi được sử dụng rộng rãi Hoạt chất dược phẩm (API) tại thuốc kê đơn chống tăng huyết áp , thuộc nhóm Chẹn thụ thể Angiotensin II (ARB) có hiệu quả trong việc ức chế angiotensin II, mang lại hiệu quả tuyệt vời giảm huyết áp và bảo vệ tim thận .
Là đối tác đáng tin cậy của bạn Nhà cung cấp nguyên liệu Valsartan , chúng tôi cung cấp nguyên liệu thô tuân thủ nghiêm ngặt theo Tiêu chuẩn dược điển USP/EP , được hỗ trợ bởi đầy đủ Tài liệu Valsartan DMF , được thiết kế đặc biệt để sản xuất các loại viên nén, viên nang chống tăng huyết áp và các công thức kết hợp (ví dụ như viên Valsartan/Hydrochlorothiazide) , giúp các công ty dược phẩm đáp ứng các yêu cầu khắt khe của thị trường toàn cầu về kiểm soát tạp chất thuốc nhóm sartan .
3. Các lĩnh vực ứng dụng chính
Thuốc kê đơn điều trị tăng huyết áp: Là thành phần dược lý chính trong thuốc chống tăng huyết áp, được sử dụng rộng rãi để sản xuất các viên nén và viên nang kê đơn nhằm điều trị tăng huyết áp vô căn.
Hỗ trợ Tiếp cận Thị trường Toàn cầu: Sản phẩm tuân thủ nhiều tiêu chuẩn dược điển và cung cấp đầy đủ hỗ trợ tài liệu đăng ký (bao gồm DMF), tạo điều kiện thuận lợi cho việc thâm nhập thị trường tại châu Âu, châu Á, Mỹ Latinh và các thị trường lớn khác trên toàn thế giới.
Công thức Phối hợp và Liệu pháp Kết hợp: Phù hợp để phát triển các công thức phối hợp với các thành phần như hydrochlorothiazide và amlodipine, tăng cường hiệu quả điều trị và sự tuân thủ của bệnh nhân.
4. Tóm tắt Giá trị Cốt lõi
Nguồn cung ổn định, Đảm bảo Sản xuất: Dựa vào các đối tác sản xuất đáng tin cậy và hệ thống chuỗi cung ứng, đảm bảo nguồn cung lâu dài và ổn định các nguyên liệu kháng tăng huyết áp, với năng lực sản xuất hàng năm vượt quá 400 tấn.
Hỗ trợ Tuân thủ, Thúc đẩy Nhanh Việc Thâm nhập Thị trường: Cung cấp đầy đủ tài liệu DMF Valsartan, hỗ trợ các hồ sơ đăng ký quốc tế như EDQM, Brazil ANVISA, Ấn Độ CDSCO, giúp rút ngắn thời gian đưa sản phẩm của bạn ra thị trường.
Logistics Toàn cầu, Giao hàng Linh hoạt: Mạng lưới logistics toàn cầu hiệu quả, hỗ trợ vận chuyển được kiểm soát hoàn toàn từ mẫu nghiên cứu và phát triển đến các đơn hàng số lượng lớn.
5. Giải pháp Trifecta
Lợi thế cung ứng nguyên liệu thô
Hỗ trợ Tuân thủ Chuyên nghiệp
Các giải pháp dịch vụ chuỗi cung ứng và hậu cần
6. Đóng gói và vận chuyển
Chúng tôi sử dụng bao bì dược phẩm đạt tiêu chuẩn, chống ẩm, chống ánh sáng, chân không hoặc đổ đầy khí nitơ, đảm bảo độ ổn định hóa học của sản phẩm trong quá trình vận chuyển và lưu trữ, đồng thời giảm thiểu nguy cơ hình thành tạp chất. Bao bì thương mại tiêu chuẩn là 25kg/thùng carton (có lớp lót túi nhựa bên trong), trong khi các mẫu nghiên cứu phát triển (R&D) và mẫu thử được cung cấp với bao bì 100g/chai hoặc 1kg/túi bạc nhôm.
7. Câu hỏi thường gặp (FAQ)
Câu hỏi: Quý vị có thể cung cấp mẫu Valsartan để xác minh chất lượng không?
A: Có. Chúng tôi cung cấp mẫu Valsartan miễn phí (thường là 100g) cho khách hàng tiềm năng, cùng với COA (Giấy chứng nhận phân tích) của lô tương ứng để xác minh kiểm tra.
Q: Giá cả và chính sách mua số lượng lớn đối với nguyên liệu Valsartan API là gì?
A: Chúng tôi cung cấp mức giá cạnh tranh cho Valsartan, với giá tốt hơn khi mua số lượng lớn. Số lượng đặt hàng tối thiểu (MOQ) và giá cụ thể vui lòng liên hệ đội ngũ bán hàng của chúng tôi. Chúng tôi cung cấp báo giá tùy chỉnh dựa trên khối lượng đặt hàng và mong muốn hợp tác dài hạn của bạn.
Hỏi: Những tài liệu chất lượng nào được cung cấp khi mua hàng?
A: Chúng tôi cung cấp COA (Giấy chứng nhận phân tích) và MSDS (Bảng dữ liệu an toàn vật liệu) kèm theo lô hàng. Tài liệu đăng ký DMF/EDMF có thể được cung cấp theo yêu cầu đối với các phần mở.
Q: Cơ chế tác động của Valsartan là gì?
A: Valsartan là một thuốc chẹn thụ thể Angiotensin II (thuốc ARB), hoạt động bằng cách ức chế tác dụng của angiotensin II, giúp giảm huyết áp, giảm gánh nặng cho tim và đạt được hiệu quả bảo vệ tim mạch.
Q: Tiêu chuẩn kiểm soát tạp chất đối với nguyên liệu Valsartan API là gì?
A: Chúng tôi tuân thủ nghiêm ngặt các tiêu chuẩn dược điển USP/EP, với sự chú ý đặc biệt đến việc kiểm soát các tạp chất nitrosamine (ví dụ: NDMA), đảm bảo độ an toàn và sự phù hợp của sản phẩm.
8. Thông số kỹ thuật Valsartan API (Tiêu chuẩn USP/EP)
Các mặt hàng |
Thông số kỹ thuật |
Ghi chú |
Mô tả |
Bột hút ẩm màu trắng hoặc gần trắng |
USP |
Độ hòa tan |
Tan tự do trong ethanol khan; ít tan trong methylene chloride; hầu như không tan trong nước |
USP |
Đánh dấu |
A. Phổ hấp thụ hồng ngoại giống hệt với phổ của chuẩn đối chiếu Valsartan |
USP |
B. Thời gian lưu của đỉnh chính trong dung dịch mẫu phải tương ứng với thời gian lưu trong dung dịch chuẩn, như thu được trong phép định lượng |
USP |
|
Độ hấp thụ |
Không quá 0,02 tại 420nm (dung dịch methanol 1/20) |
USP |
Nước |
Không quá 2,0% |
USP |
Azide |
Không quá 4,7 ppm |
Chuẩn nội |
Các hợp chất liên quan |
Hợp chất liên quan A: Không nhiều hơn 1,0% |
USP |
Hợp chất liên quan B: Không nhiều hơn 0,2% | ||
Hợp chất liên quan C: Không nhiều hơn 0,1 % | ||
Bất kỳ tạp chất cá thể nào khác: Không nhiều hơn 0,10% | ||
Tổng tạp chất (không bao gồm hợp chất liên quan A ): Không nhiều hơn 0,3% | ||
Các dung môi Còn lại |
Methanol: Không nhiều hơn 3000ppm |
Chuẩn nội |
Ethyl acetate: Không nhiều hơn 5000ppm | ||
Methylene chloride: Không nhiều hơn 600ppm | ||
Toluene: Không nhiều hơn 890ppm | ||
N,N-Dimethylformamide: Không nhiều hơn 880ppm | ||
Tàn dư khi đốt |
Không quá 0,1 % |
USP |
Phân bố kích thước hạt |
Tham khảo |
Theo yêu cầu của khách hàng |
Mật độ khối lượng |
Tham khảo |
Theo yêu cầu của khách hàng |
Mật độ đổ đầy |
Tham khảo |
Theo yêu cầu của khách hàng |
Phân tích hàm lượng |
98,0%---102,0% của C₂₄H₂₉N₅O₃ tính theo cơ sở khan nước |
USP |
N-Nitroso- |
Chuẩn nội |
|
N-Nitrosodiethyla |
Chuẩn nội |
|
Azidosartan Biphenyl |
Không quá 4,7 ppm |
Chuẩn nội |
Azidosartan Biphenyl Tetrazolium |
Không quá 4,7 ppm |
Chuẩn nội |
Dạng tinh thể |
Các vị trí đỉnh trong phổ XRPD của sản phẩm này tương ứng với các vị trí đã được báo cáo cho dạng chủ yếu vô định hình trong Bằng sáng chế US7105557B2. |
Theo yêu cầu của khách hàng |
Giới hạn vi sinh |
Không quá 10 cfu tổng số vi sinh vật hiếu khí trong 1 g mẫu; không quá 10² cfu tổng số nấm men và nấm mốc kết hợp trong 1 g mẫu; Escherichia coli không có trong 1 g mẫu. |
* |
Tiêu chuẩn đã thiết lập |
Tiêu chuẩn nội bộ đã được thiết lập theo chuyên luận USP cho Valsartan |
|
9. Liên hệ chúng tôi
Đang tìm kiếm đối tác chiến lược trong lĩnh vực thuốc điều trị tim mạch?
GTIG Guomian là đối tác lý tưởng trong chuỗi cung ứng nguyên liệu Valsartan của bạn.
Liên hệ ngay để nhận giải pháp tùy chỉnh và mẫu thử miễn phí!
Ngày phát hành tài liệu: 7 tháng 1 năm 2026
© 2026 GTIG Guomian – Nhà cung cấp chuyên nghiệp nguyên liệu API dược phẩm và hóa chất đặc dụng