Valsartán
Bloqueante de receptores de angiotensina II de alta pureza para el tratamiento de la hipertensión
GTIG Guomian es su Proveedor de API de Valsartán y socio estratégico. Nos especializamos en suministrar productos de alta pureza API bloqueantes de receptores de angiotensina II cumple con Estándares farmacopeicos USP/EP , adecuado para fármaco antihipertensivo y producto para el tratamiento cardiovascular desarrollo.
Nuestros productos provienen de instalaciones cGMP certificadas, respaldadas por documentación completa Documentación de Valsartan DMF , asegurando un suministro estable a los mercados globales.
- Resumen
- Productos recomendados
- Aseguramiento de calidad: Control estricto bajo nuestro sistema de calidad cGMP, con especial atención al control de impurezas de nitrosaminas (por ejemplo, NDMA) , garantizando estándares de seguridad y consistencia de calidad para cada lote.
- Capacidad de producción estable: Contamos con socios de producción confiables y cadenas de suministro optimizadas, asegurando eficazmente a largo plazo, estable el suministro de este API cardiovascular crítico. (La capacidad anual de producción supera las 400 toneladas)
- Flexibilidad de Especificaciones: Ofrecemos múltiples especificaciones, desde 100 g de grado I+D, muestras de 1 kg hasta embalajes comerciales de 25 kg, satisfaciendo sus diferentes necesidades en las distintas etapas, desde I+D hasta producción comercial.
- Documentación Técnica Completa: Cada lote de pRODUCTOS viene acompañado de Certificado de Análisis (COA) y Ficha de Datos de Seguridad del Material (MSDS) , incluidos informes detallados de pruebas de impurezas nitrosaminas .
- Soporte de Documentación para Registro: Podemos proporcionar a socios calificados partes abiertas de la documentación DMF/EDMF necesarias para el registro de medicamentos en EE. UU., la UE y otros mercados internacionales, acelerando significativamente su proceso de registro de productos.
- Consulta Regulatoria: Nuestro equipo de asuntos regulatorios puede ofrecer consultoría sobre los últimos requisitos regulatorios para medicamentos sartánicos en mercados objetivo (por ejemplo, Brasil ANVISA, India CDSCO).
- Asociación con empresas profesionales de logística química que cubren mercados clave como Europa, Asia-Pacífico y América Latina.
- Dominio de los procedimientos de despacho aduanero, proporcionando seguimiento completo de carga y compromisos de entrega.
1. Resumen del Producto Principal
|
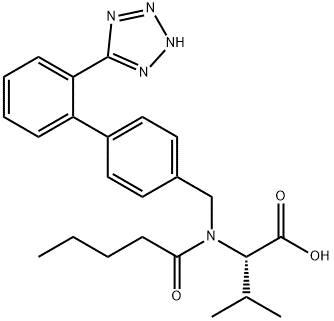
Nombre del producto: Valsartán Nº CAS: 137862-53-4 Fórmula molecular: C ₂₄ H ₂₉ N ₅ O 3. Peso molecular: 435.52 |
 |
Grado/Estándar: Grado farmacéutico, conforme con los estándares USP/EP
Apariencia: Polvo cristalino blanco a blanco amarillento
Cantidad mínima de pedido: 100g (I+D), 1kg (muestra), 25kg (pedidos comerciales, LCL soportado)
2. Descripción general del producto
Valsartán es un núcleo ampliamente utilizado Ingrediente Farmacéutico Activo (API) en medicamentos recetados antihipertensivos , perteneciente a la Clase de bloqueadores del receptor de angiotensina II (ARB) clase. Bloquea eficazmente la angiotensina II, proporcionando excelentes reducción de la presión arterial y protección cardiorenal .
Como su confiable Proveedor de API de Valsartán , proporcionamos materias primas estrictamente conformes con Estándares farmacopeicos USP/EP , respaldado por un completo Documentación de Valsartan DMF , diseñado específicamente para la producción de medicamentos de alta calidad comprimidos antihipertensivos, cápsulas y formulaciones combinadas (como comprimidos de Valsartán/Hidroclorotiazida) , ayudando a las compañías farmacéuticas a cumplir con los rigurosos requisitos del mercado global para el control de impurezas en medicamentos sartanes .
3. Áreas Principales de Aplicación
Medicamentos Antihipertensivos Recetados: Como ingrediente principal en medicamentos antihipertensivos, ampliamente utilizado en la producción de comprimidos y cápsulas recetados para el tratamiento de la hipertensión esencial.
Soporte para el acceso a mercados globales: Los productos cumplen con múltiples estándares farmacopeicos y ofrecen soporte completo de documentación para registro (incluyendo DMF), facilitando la entrada al mercado en Europa, Asia, América Latina y otros principales mercados mundiales.
Formulaciones combinadas y terapia combinada: Adecuado para desarrollar formulaciones combinadas con componentes como hidroclorotiazida y amlodipino, mejorando la eficacia terapéutica y la adherencia del paciente.
4. Resumen de Valor Principal
Suministro estable, asegurando la producción: Contamos con socios productores confiables y sistemas de cadena de suministro que garantizan un suministro estable a largo plazo de principios activos antihipertensivos, con una capacidad de producción anual superior a las 400 toneladas.
Soporte de cumplimiento, acelerando la entrada al mercado: Proporcionamos documentación completa de DMF de Valsartán, apoyando presentaciones internacionales de registro como EDQM, ANVISA de Brasil y CDSCO de India, ayudando a reducir el tiempo de comercialización de su producto.
Logística global, entrega flexible: Red logística global eficiente, que respalda el transporte completamente controlado desde muestras de I+D hasta pedidos masivos.
5. Solución Trifecta
Ventajas en el suministro de materias primas
Soporte Profesional de Cumplimiento
Soluciones de servicios de cadena de suministro y logística
6. Embalaje y transporte
Utilizamos empaques farmacéuticos resistentes a la humedad, a la luz, al vacío o rellenos de nitrógeno, asegurando la estabilidad química del producto durante el transporte y almacenamiento, y minimizando los riesgos de formación de impurezas. El empaque comercial estándar es de 25 kg/tambor de cartón (con bolsa interior de plástico), mientras que para I+D y muestras se proporcionan envases de 100 g/frasco o 1 kg/bolsa de lámina de aluminio.
7. Preguntas frecuentes (FAQ)
P: ¿Pueden proporcionar muestras de Valsartán para verificación de calidad?
Sí. Proporcionamos muestras gratuitas de Valsartán (típicamente 100 g) a clientes potenciales, junto con el COA (Certificado de Análisis) del lote correspondiente para verificación mediante pruebas.
P: ¿Cuál es el precio y la política de compra por volumen para el API de Valsartán?
R: Ofrecemos precios competitivos para Valsartán, con mejores condiciones para compras al por mayor. Para conocer la CMC (Cantidad Mínima de Pedido) específica y los precios, consulte a nuestro equipo de ventas. Proporcionamos cotizaciones personalizadas según su volumen de compra e intención de cooperación a largo plazo.
P: ¿Qué documentos de calidad se proporcionan al realizar la compra?
R: Proporcionamos COA (Certificado de Análisis) y MSDS (Hoja de Datos de Seguridad de Materiales) junto con los envíos. La documentación de registro DMF/EDMF puede proporcionarse bajo solicitud para partes abiertas.
P: ¿Cuál es el mecanismo de acción del Valsartán?
R: El Valsartán es un bloqueador de los receptores de angiotensina II (fármaco ARB) que actúa bloqueando la acción de la angiotensina II, reduciendo la presión arterial, disminuyendo la carga cardíaca y logrando una protección cardiovascular.
P: ¿Cuáles son los estándares de control de impurezas para el API de Valsartán?
A: Seguimos estrictamente los estándares farmacopeicos USP/EP, prestando especial atención al control de impurezas de nitrosaminas (por ejemplo, NDMA), garantizando la seguridad y conformidad del producto.
8. Parámetros técnicos del API Valsartan (especificaciones USP/EP)
Artículos |
ESPECIFICACIÓN |
Observaciones |
Descripción |
Polvo hidroscópico blanco o casi blanco |
USP |
Solubilidad |
Soluble libremente en etanol anhidro; ligeramente soluble en cloruro de metileno; prácticamente insoluble en agua |
USP |
Identificación |
A. El espectro de absorción infrarroja es idéntico al del estándar de referencia de Valsartan |
USP |
B. El tiempo de retención del pico principal de la solución de la muestra corresponde al de la solución patrón, obtenido en el ensayo |
USP |
|
Absorción |
No más de 0.02 a 420 nm (solución 1/20 en metanol) |
USP |
Agua |
No más del 2.0% |
USP |
Azida |
No más de 4.7 ppm |
Estándar interno |
Compuestos relacionados |
Compuesto relacionado A: No más del 1,0 % |
USP |
Compuesto relacionado B: No más del 0,2 % | ||
Compuesto relacionado C: No más del 0,1 % | ||
Cualquier otra impureza individual: No más del 0,10 % | ||
Impurezas totales (excluyendo el compuesto relacionado A ): No más del 0,3 % | ||
Disolventes residuales |
Metanol: No más de 3000 ppm |
Estándar interno |
Acetato de etilo: No más de 5000 ppm | ||
Cloruro de metileno: No más de 600 ppm | ||
Tolueno: No más de 890 ppm | ||
N,N-Dimetilformamida: No más de 880 ppm | ||
Residuo tras Ignición |
No más del 0,1 % |
USP |
Distribución del tamaño de partículas |
Referencia |
Según solicitado por el cliente |
Densidad a granel |
Referencia |
Según solicitado por el cliente |
Densidad apisonada |
Referencia |
Según solicitado por el cliente |
Análisis |
98,0 % --- 102,0 % de C₂₄H₂₉N₅O₃ calculado sobre base anhidra |
USP |
N-Nitroso- |
Estándar interno |
|
N-Nitrosodietilamina |
Estándar interno |
|
Azidosartán Bifenilo |
No más de 4.7 ppm |
Estándar interno |
Azidosartán Bifenilo Tetrazolio |
No más de 4.7 ppm |
Estándar interno |
Forma cristalina |
Las posiciones máximas en el patrón XRPD de este producto corresponden a las indicadas para la forma predominantemente amorfa en la patente US7105557B2. |
Según solicitado por el cliente |
Límite microbiano |
No más de 10 ufc de recuento microbiano aerobio total en 1 g de la muestra; no más de 10² ufc de recuento total combinado de levaduras y mohos en 1 g de la muestra; Escherichia coli ausente en 1 g de la muestra. |
* |
Estándar establecido |
El estándar interno se estableció de acuerdo con el monográfico de la USP para Valsartán |
|
9. Contáctenos
¿Busca un socio estratégico en medicamentos para el tratamiento cardiovascular?
GTIG Guomian es su socio ideal en la cadena de suministro de API de Valsartán.
¡Contáctenos ahora para soluciones personalizadas y muestras gratuitas!
Fecha de generación del documento: 7 de enero de 2026
© 2026 GTIG Guomian – Proveedor profesional de API farmacéuticos y productos químicos especiales