Valsartan
Bloquant de récepteurs de l'angiotensine II à haute pureté pour le traitement de l'hypertension
GTIG Guomian est votre solution fiable. Fournisseur d'ingrédient actif Valsartan et partenaire stratégique. Nous sommes spécialisés dans la fourniture de principes actifs Bloquants des récepteurs de l'angiotensine II à haute pureté conforme aux normes Normes pharmacopée USP/EP , adapté pour médicament antihypertenseur et produit de traitement cardiovasculaire innovation.
Nos produits proviennent d'installations cGMP certifiées, soutenues par un dossier complet Documentation DMF du valsartan , assurant une fourniture stable aux marchés mondiaux.
- Aperçu
- Produits recommandés
- Assurance qualité : Contrôle strict dans le cadre de notre système qualité cGMP, avec une attention particulière portée à la maîtrise des impuretés nitrosamines (par exemple, NDMA) , garantissant les normes de sécurité et la constance de qualité pour chaque lot.
- Capacité de production stable : Nous disposons de partenaires de production fiables et de chaînes d'approvisionnement optimisées, assurant efficacement à long terme, stable l'approvisionnement de cet API cardiovasculaire essentiel. (La capacité annuelle de production dépasse 400 tonnes)
- Flexibilité des caractéristiques techniques : Nous proposons plusieurs spécifications allant de l'échelle R&D (100 g), aux échantillons de 1 kg jusqu'à l'emballage commercial de 25 kg, répondant ainsi à vos besoins à chaque étape, de la R&D à la production commerciale.
- Documentation technique complète : Chaque lot de produits est fourni avec une documentation détaillée Certificat d'analyse (COA) et Fiche de données de sécurité (MSDS) , y compris rapports d'analyse sur les impuretés nitrosamines .
- Soutien pour la documentation d'enregistrement : Nous pouvons fournir aux partenaires qualifiés les parties ouvertes de la documentation DMF/EDMF nécessaires à l'enregistrement des médicaments aux États-Unis, en Europe et sur d'autres marchés internationaux, accélérant ainsi considérablement votre processus d'enregistrement.
- Consultation réglementaire : Notre équipe des affaires réglementaires peut fournir une consultation sur les dernières exigences réglementaires applicables aux médicaments sartans dans les marchés cibles (par exemple, Brésil ANVISA, Inde CDSCO).
- Partenariat avec des entreprises spécialisées en logistique chimique couvrant des marchés clés tels que l'Europe, l'Asie-Pacifique et l'Amérique latine.
- Expérimentés dans les procédures de dédouanement, nous offrons un suivi complet des cargaisons et nous engageons sur les délais de livraison.
1. Résumé du produit principal
|
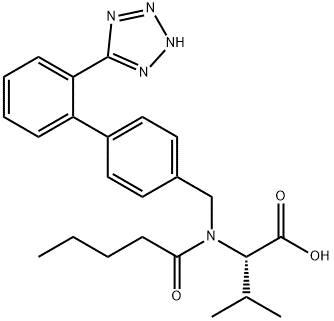
Nom du produit : Valsartan N° CAS : 137862-53-4 Formule moléculaire : C ₂₄ H ₂₉ N ₅ O ₃ Poids moléculaire: 435.52 |
 |
Grade/Norme : Qualité pharmaceutique, conforme aux normes USP/EP
Apparence : Poudre cristalline de blanc à crème
Quantité minimale de commande : 100g (R&D), 1kg (échantillon), 25kg (commandes commerciales, LCL pris en charge)
2. Aperçu du produit
Valsartan est un noyau largement utilisé Principe Actif Pharmaceutique (API) sur médicaments d'ordonnance antihypertenseurs , appartenant à la Classe des bloqueurs des récepteurs de l'angiotensine II (ARB) classe. Il bloque efficacement l'angiotensine II, offrant un excellent réduction de la pression artérielle et protection cardiorénale .
En tant que votre partenaire fiable Fournisseur d'ingrédient actif Valsartan , nous fournissons des matières premières strictement conformes à Normes pharmacopée USP/EP , soutenues par un ensemble complet de Documentation DMF du valsartan , conçues spécifiquement pour la production de comprimés, gélules et formules combinées antihypertenseurs (tels que les comprimés de Valsartan/Hydrochlorothiazide) , aidant les entreprises pharmaceutiques à répondre aux exigences strictes des marchés mondiaux en matière de contrôle des impuretés dans les médicaments sartans .
3. Domaines d'application principaux
Médicaments antihypertenseurs sur ordonnance : En tant qu'ingrédient actif antihypertenseur principal, largement utilisé dans la fabrication de comprimés et de gélules sur ordonnance destinés au traitement de l'hypertension essentielle.
Support pour l'accès aux marchés mondiaux : Les produits sont conformes à plusieurs normes pharmacopée et offrent un support complet pour la documentation d'enregistrement (y compris le DMF), facilitant l'entrée sur les marchés européens, asiatiques, latino-américains et autres principaux marchés mondiaux.
Formulations combinées et thérapie combinée : Adapté au développement de formulations combinées avec des composants tels que l'hydrochlorothiazide et l'amlodipine, améliorant ainsi l'efficacité thérapeutique et l'observance par le patient.
4. Résumé des valeurs clés
Approvisionnement stable, garantissant la production : S'appuyant sur des partenaires de production fiables et des systèmes de chaîne d'approvisionnement robustes, assurant un approvisionnement à long terme stable en principes actifs antihypertenseurs, avec une capacité de production annuelle dépassant 400 tonnes.
Support de conformité, accélérant l'entrée sur le marché : Fourniture d'un dossier DMF complet pour le valsartan, soutenant les dépôts d'enregistrement internationaux auprès d'organismes tels que l'EDQM, l'ANVISA au Brésil, le CDSCO en Inde, contribuant ainsi à réduire le délai de mise sur le marché de votre produit.
Logistique mondiale, livraison flexible : Réseau logistique mondial efficace, prenant en charge un transport entièrement contrôlé des échantillons de R&D aux commandes en vrac.
5. Solution Trifecta
Avantages de l'approvisionnement en matières premières
Soutien professionnel en matière de conformité
Solutions de services logistiques et de chaîne d'approvisionnement
6. Emballage et transport
Nous utilisons des emballages pharmaceutiques résistants à l'humidité, à la lumière, sous vide ou remplis d'azote, garantissant la stabilité chimique du produit pendant le transport et le stockage, et minimisant les risques de formation d'impuretés. L'emballage commercial standard est de 25 kg/tonneau en carton (avec doublure interne en sac plastique), tandis que les produits destinés à la R&D et les échantillons sont fournis en flacon de 100 g ou en sachet en aluminium de 1 kg.
7. Questions fréquemment posées (FAQ)
Q : Pouvez-vous fournir des échantillons de Valsartan pour vérification de la qualité ?
A : Oui. Nous fournissons gratuitement des échantillons de Valsartan (généralement 100 g) aux clients potentiels, accompagnés du COA (certificat d'analyse) correspondant au lot pour la vérification des tests.
Q : Quel est le prix et la politique d'achat en gros pour l'API Valsartan ?
A : Nous proposons des prix compétitifs pour le Valsartan, avec des tarifs plus avantageux pour les achats en gros. Pour connaître les quantités minimales de commande (MOQ) et les prix spécifiques, veuillez consulter notre équipe commerciale. Nous établissons des devis personnalisés en fonction de votre volume d'achat et de vos intentions de coopération à long terme.
Q : Quels documents relatifs à la qualité sont fournis lors de l'achat ?
A : Nous fournissons un COA (certificat d'analyse) et une FDS (fiche de données de sécurité) avec chaque expédition. La documentation d'enregistrement DMF/EDMF peut être fournie sur demande pour les parties ouvertes.
Q : Quel est le mécanisme d'action du Valsartan ?
A : Le Valsartan est un bloqueur des récepteurs de l'angiotensine II (médicament de la classe des ARA) qui agit en bloquant l'action de l'angiotensine II, abaissant ainsi la pression artérielle, réduisant la charge de travail du cœur et assurant une protection cardiovasculaire.
Q : Quelles sont les normes de contrôle des impuretés pour l'API Valsartan ?
A : Nous suivons strictement les normes pharmacopée USP/EP, en accordant une attention particulière au contrôle des impuretés nitrosamines (par exemple, NDMA), garantissant ainsi la sécurité et la conformité du produit.
8. Paramètres techniques de l'ingrédient pharmaceutique actif Valsartan (spécifications USP/EP)
Articles |
Spécification |
Remarques |
Description |
Poudre hygroscopique blanche ou presque blanche |
USP |
Solubilité |
Très soluble dans l'éthanol anhydre ; peu soluble dans le chlorure de méthylène ; pratiquement insoluble dans l'eau |
USP |
Identification |
A. Le spectre d'absorption infrarouge est identique à celui de l'étalon de référence du Valsartan |
USP |
B. Le temps de rétention du pic principal de la solution échantillon correspond à celui de la solution étalon, tel qu'obtenu lors du dosage |
USP |
|
Absorbance |
Pas plus de 0,02 à 420 nm (solution 1/20 dans le méthanol) |
USP |
Eau |
Pas plus de 2,0 % |
USP |
Azoture |
Pas plus de 4,7 ppm |
Étalon interne |
Composés apparentés |
Composé apparenté A : Pas plus de 1,0 % |
USP |
Composé apparenté B : Pas plus de 0,2 % | ||
Composé apparenté C : Pas plus de 0,1 % | ||
Toute autre impureté individuelle : Pas plus de 0,10 % | ||
Impuretés totales (à l'exclusion du composé apparenté A ): Pas plus de 0,3 % | ||
Solvants résiduels |
Méthanol : Pas plus de 3000 ppm |
Étalon interne |
Acétate d'éthyle : Pas plus de 5000 ppm | ||
Chlorure de méthylène : Pas plus de 600 ppm | ||
Toluène : Pas plus de 890 ppm | ||
N,N-Diméthylformamide : Pas plus de 880 ppm | ||
Résidu après ignition |
Pas plus de 0,1 % |
USP |
Répartition des tailles de particules |
Référence |
Tel que demandé par le client |
Densité de masse |
Référence |
Tel que demandé par le client |
Densité en vrac |
Référence |
Tel que demandé par le client |
Teneur |
98,0 % --- 102,0 % de C₂₄H₂₉N₅O₃ calculé sur une base anhydre |
USP |
N-Nitroso- |
Étalon interne |
|
N-Nitrosodiéthylamine |
Étalon interne |
|
Azidosartan Biphenyle |
Pas plus de 4,7 ppm |
Étalon interne |
Azidosartan Biphenyle Tétrazolium |
Pas plus de 4,7 ppm |
Étalon interne |
Forme cristalline |
Les pics de position dans le spectre XRPD de ce produit correspondent à ceux indiqués pour la forme principalement amorphe dans le brevet US7105557B2. |
Tel que demandé par le client |
Limite microbienne |
Pas plus de 10 ufc de comptage total des micro-organismes aérobies par gramme d'échantillon ; pas plus de 10² ufc de comptage total combiné des levures et des moisissures par gramme d'échantillon ; absence d'Escherichia coli dans 1 g d'échantillon. |
* |
Norme établie |
La norme interne a été établie conformément à la monographie USP du valsartan |
|
9. Contactez-nous
Vous recherchez un partenaire stratégique dans les médicaments pour le traitement cardiovasculaire ?
GTIG Guomian est votre partenaire idéal pour la chaîne d'approvisionnement en principe actif de valsartan.
Contactez-nous dès maintenant pour des solutions personnalisées et des échantillons gratuits !
Date de génération du document : 7 janvier 2026
© 2026 GTIG Guomian – Fournisseur professionnel d'API pharmaceutiques et de produits chimiques spécialisés